 1645
2021-08-13
1645
2021-08-13
颗粒在线讯:利用两性烯丙基金属络合物实现亲电和亲核烯丙基化反应,是有机合成中重要的碳碳键合成方法。两性烯丙基金属络合物催化的不对称亲电烯丙基化反应得到广泛研究,而利用极性翻转策略,通过两性烯丙基金属络合物亲核性反应模式,实现不对称烯丙基化反应的报道较少。手性高烯丙醇是具有生物活性的药物分子和天然产物中常见结构片段。金属催化醛的不对称烯丙基化反应已有较多报道,但缺乏利用简单易得的手性金属络合物,通过高多样性的烯丙基前体,实现高立体选择性的广泛底物适用性的不对称烯丙基化方法。因此,亟须开发出利用烯丙基钴络合物通过极性翻转的策略实现不对称反应构建手性高烯丙醇的新方法。
中国科学院上海有机化学研究所金属有机化学国家重点实验室孟繁柯课题组致力于钴催化的不对称反应研究。前期研究中,孟繁柯课题组发展了一系列钴催化新型不对称反应(Angewandte Chemie International Edition, 2019, 58, 11049-11053;Angewandte Chemie International Edition, 2021, 60, 2694-2698;Cell Reports Physical Science, 2021, 2, 100406)。近日,该课题组在探索烯丙基钴的化学反应过程中,利用极性翻转策略,发现通过烯丙基自由基中间体与醛发生高立体选择性的立体汇聚式加成反应,取得了新的研究进展。(Journal of the American Chemical Society,DOI: 10.1021/jacs.1c05690)
研究表明,通过原位还原产生一价钴络合物,可以与烯丙醇及多种衍生物发生氧化加成,产生的烯丙基钴中间体可以发生均裂,生成烯丙基自由基,其发生快速异构化,使原料烯丙醇衍生物的立体化学不会转移到产物中,从而实现立体汇聚式反应模式。进一步研究发现,烯丙基二价钴是发生亲核反应的中间体。该反应产率和立体选择性优异,底物适用性广泛,可兼容多种敏感官能团,通过手性钴络合物单一的催化平台,实现具有叔碳和季碳中心的不对称烯丙基化反应,解决了不对称烯丙基化反应领域长期无法解决的问题。反应产物进行后续官能团转化,可以高效构建生物活性分子,该方法被应用于天然产物paliclavine骨架的构建。
研究工作得到国家自然科学基金委员会、上海市科学技术委员会、中科院、上海有机所和金属有机化学国家重点实验室的支持。
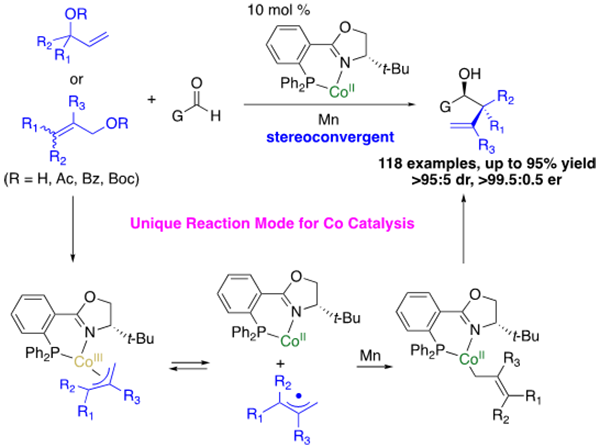
催化不对称烯丙位碳氢官能团化反应
版权与免责声明:
(1) 凡本网注明"来源:颗粒在线"的所有作品,版权均属于颗粒在线,未经本网授权不得转载、摘编或利用其它方式使用上述作品。已获本网授权的作品,应在授权范围内使用,并注明"来源:颗粒在线"。违反上述声明者,本网将追究相关法律责任。
(2)本网凡注明"来源:xxx(非颗粒在线)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
(3)如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。